- Историческая справка
- Понятие окислительно-восстановительной реакции
- Важнейшие окислители и восстановители
- Классификация
- Составление уравнении окислительно-восстановительных реакции
- Метод электронного баланса
- Метод полуреакций, или ионно-электронный метод
- Основные схемы окислительно-восстановительных реакций
- Взаимодействие металлов с серной кислотой
- Схема восстановления перманганатов
- Азотистая кислота и нитриты
- Пероксид водорода
- Окислительные свойства азотной кислоты
- Схема восстановления хроматов/бихроматов
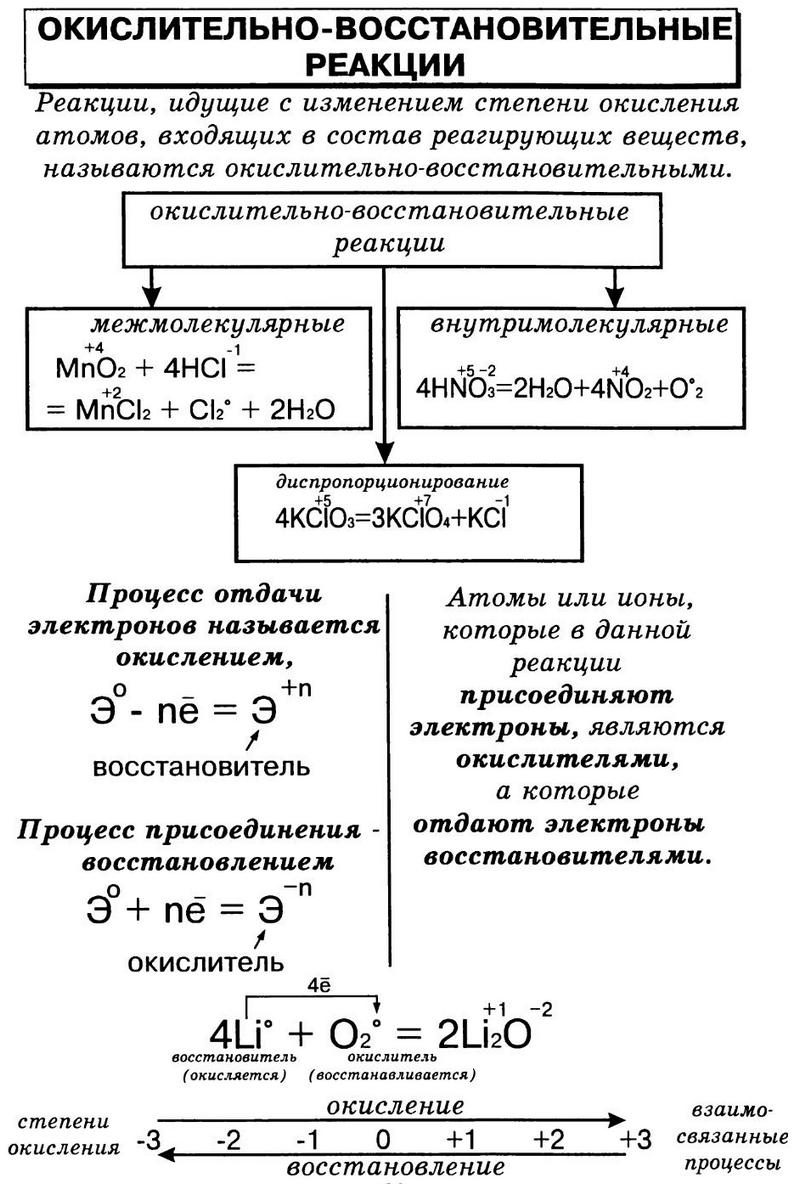
Историческая справка
Издавна учёные полагали, что окисление — потеря флогистона (особого невидимого горючего вещества, термин которого ввел Иоганн Бехер), а восстановление — его приобретение. Но, после создания А. Лавуазье в 1777 году кислородной теории горения, к началу XIX века химики стали считать окислением взаимодействие веществ с кислородом, а восстановлением их превращения под действием водорода. Тем не менее в качестве окислителя могут выступать и другие элементы, например
В соответствии с электронно-ионной теорией окисления-восстановления, разработанной Л. В. Писаржевским в 1914 г., окисление — процесс отщепления электронов от атомов или ионов элемента, который окисляется; Восстановлением называется процесс присоединения электронов к атомам или ионам элемента, каковой восстанавливается. Например, в реакции атом цинка теряет два электрона, то есть окисляется, а молекула хлора присоединяет их, то есть восстанавливается.
Понятие окислительно-восстановительной реакции
Окислительно-восстановительные реакции (ОВР) – это процессы, в ходе которых изменяются степени окисления атомов химических элементов.
Окисление и восстановление сопровождают друг друга. Один процесс без другого просто не существует. Почему?
Изменение степени окисления всегда означает переход электронов от одних частиц к другим. То есть одни частицы отдают электроны в ходе химического или электрохимического взаимодействия, а другие частицы принимают. Здесь срабатывает закон сохранения материи .
Важнейшие окислители и восстановители
Какие вещества могут проявлять свойства окислителей, а какие — восстановителей? Как уже говорилось, окислитель содержит в своем составе элемент, понижающий степень своей окисленности, а восстановитель содержит элемент, степень окисленности которого повышается в ходе реакции. Следовательно, окислителями могут быть прежде всего соединения высших, а восстановителями — низших степенен окисленности, присущих данному элементу.
Металлы проявляют в своих соединениях только положительную окисленность, и низшая их степень окисленности равна нулю. Иначе говоря, низшей степенью окисленности они обладают только в свободном состоянии. Действительно, все свободные металлы способны, хотя и в различной степени, проявлять только восстановительные свойства. На практике в качестве восстановителей применяют алюминий, магний, натрий, калий, цинк и некоторые другие металлы. Если металлу присущи несколько степеней окисленности, то те его соединения, в которых он проявляет низшую из них, также обычно являются восстановителями, например, соединения железа(II), олова(II), хрома(II), меди(I).
Окислителями могут быть те соединения металлов, в которых степень окисленности металла велика — равна номеру группы, в которой находится металл, или близка к нему. На практике применяют, в частности: аммиачный раствор оксида серебра, аммиачный раствор сульфата меди(II), хлорид ртути(II), диоксид свинца.
Неметаллы проявляют как положительную, так и отрицательную окисленность. Естественно, что соединения, содержащие неметаллы в высших положительных степенях окисленности, могут быть окислителями, а соединения, в которых неметалл проявляет отрицательную окисленность, — восстановителями.
К широко применяемым в промышленности восстановителям относятся водород, углерод (в виде угля или кокса) и монооксид углерода 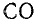 .
.
К сильным окислителям принадлежат неметаллы верхней части VI и VII групп периодической системы. Сильные окислительные свойства этих веществ объясняются большой электроотрицательностью их атомов. Сильнее всего окислительные свойства выражены у фтора, но в практике чаще пользуются в качестве окислителей кислородом, хлором и бромом.
К соединениям, применяемым в качестве окислителей, относятся также кислоты. Наибольшее практическое значение имеют соляная, серная и азотная кислоты. При этом элементом окислителем в соляной кислоте является водород, в азотной — азот, в разбавленной серной — водород, в концентрированной — сера. Поэтому уравнение процесса восстановления соляной и разбавленной серной кислот имеет вид:
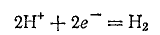
Азотная кислота, в зависимости от ее концентрации, температуры и природы восстановителя, может восстанавливаться до различных степеней окисленности азота. Одним из обычных продуктов ее восстановления является оксид азота 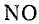 :
:
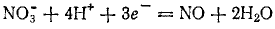
При восстановлении концентрированной серной кислоты также могут образовываться различные продукты. Одним из них может быть диоксид серы:
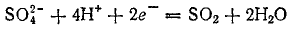
Из других соединений неметаллов, применяемых в качестве окислителей, можно указать на пероксид водорода, соли кислот, в которых кислотообразующий элемент проявляет высокую степень окисленности — хлораты 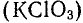 , перхлораты
, перхлораты 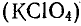 .
.
Классификация
Выделяют четыре вида ОВР:
- межмолекулярные – атомы окислителя и восстановителя находятся в молекулах разных веществ: MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O;
- внутримолекулярные – атомы окислителя и восстановителя входят в состав одного и того же вещества: 2KClO3 = 2KCl + 3O2;
- диспропорционирования или самоокисления-самовосстановления – атом одного и того же элемента выполняет функцию и восстановителя, и окислителя: 4K2SO3 = 3K2SO4 + K2S (в K2SO4 сера – восстановитель, в K2S – окислитель);
- контрпропорционирования – атомы одного элемента в составе исходных веществ имеют разные степени окисления, а конечных – одинаковую: S+4O2 + 2H2S+2 = 3S0 + 2H2O.
Процесс окисления (отдачи электронов) записывают со знаком минус, показывая, сколько электронов получил окислитель: S-2 – 2ē → S0, Al0 – 3ē → Al+3, Fe+2 – ē → Fe+3. Процесс восстановления (присоединения электронов) записывается со знаком плюса: Mn+4 + 2ē → Mn+2, S0 + 2ē → S-2, Cr+6 + 3ē → Cr+3.

Составление уравнении окислительно-восстановительных реакции
Применяются два метода составления уравнений окислительно-восстановительных реакций — метод электронного баланса и метод полуреакций.
Метод электронного баланса
В этом методе сравнивают степени окисления атомов в исходных и конечных веществах, руководствуясь правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединенных окислителем. Для составления уравнения надо знать формулы реагирующих веществ и продуктов реакции. Последние определяются либо опытным путем, либо на основе известных свойств элементов. Рассмотрим применение этого метода на примерах.
Пример 1. Составление уравнения реакции меди с раствором нитрата палладия (II). Запишем формулы исходных и конечных веществ реакции и покажем изменения степеней окисления:
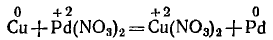
Медь, образуя ион меди, отдает два электрона, ее степень окисления повышается от 0 до +2. Медь — восстановитель. Ион палладия, присоединяя два электрона, изменяет степень окисления от +2 до 0. Нитрат палладия (II) — окислитель. Эти изменения можно выразить электронными уравнениями
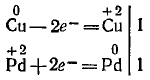
из которых следует, что при восстановителе и окислителе коэффициенты равны 1. Окончательное уравнение реакции:
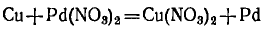
Как видно, в суммарном уравнении реакции электроны не фигурируют.
Чтобы проверить правильность составленного уравнения, подсчитываем число атомов каждого элемента в его правой и левой частях. Например, в правой части 6 атомов кислорода, в левой также 6 атомов; палладия 1 и 1; меди тоже 1 и 1. Значит, уравнение составлено правильно.
Переписываем это уравнение в ионной форме:
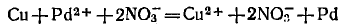
И после сокращения одинаковых ионов получим
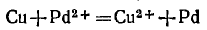
Пример 2. Составление уравнения реакции взаимодействия оксида марганца (IV) с концентрированной соляной кислотой (с помощью этой реакции в лабораторных условиях получают хлор). Запишем формулы исходных и конечных веществ реакции:
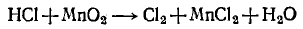
Покажем изменение степеней окисления атомов до и после реакции:
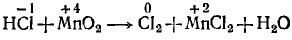
Эта реакция окислительно-восстановительная, так как изменяются степени окисления атомов хлора и марганца. HCl — восстановитель, МnO2 — окислитель. Составляем электронные уравнения:
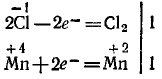
и находим коэффициенты при восстановителе и окислителе. Они соответственно равны 2 и 1. Коэффициент 2 (а не 1) ставится потому, что 2 атома хлора со степенью окисления — 1 отдают 2 электрона. Этот коэффициент уже стоит в электронном уравнении:
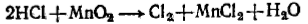
Находим коэффициенты для других реагирующих веществ. Из электронных уравнений видно, что на 2 моль НСl приходится 1 моль МnО2. Однако, учитывая, что для связывания образующегося двухзарядного иона марганца нужно еще 2 моль кислоты, перед восстановителем следует поставить коэффициент 4. Тогда воды получится 2 моль. Окончательное уравнение имеет вид
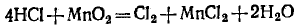
Проверку правильности написания уравнения можно ограничить подсчетом числа атомов одного какого-либо элемента, например хлора: в левой части 4 и в правой 2+2=4.
Поскольку в методе электронного баланса изображаются уравнения реакций в молекулярной форме, то после составления и проверки их следует написать в ионной форме. Перепишем составленное уравнение в ионной форме:
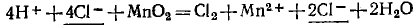
и после сокращения одинаковых ионов в обеих частях уравнения (они подчеркнуты) получим
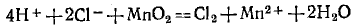
Пример 3. Составление уравнения реакции взаимодействия сероводорода с подкисленным раствором перманганата калия. Напишем схему реакции — формулы исходных и полученных веществ:
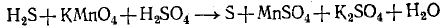
Затем покажем изменение степеней окисления атомов до и после реакции:
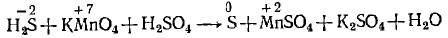
Изменяются степени окисления у атомов серы и марганца (H2S — восстановитель, КMnO4 — окислитель). Составляем электронные уравнения, т. е. изображаем процессы отдачи и присоединения электронов:
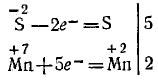
И наконец, находим коэффициенты при окислителе и восстановителе, а затем при других реагирующих веществах. Из электронных уравнений видно, что надо взять 5 моль H2S и 2 моль КMnO4, тогда получим 5 моль атомов S и 2 моль КMnO4. Кроме того, из сопоставления атомов в левой и правой частях уравнения, найдем, что образуется также 1 моль K2SO4 и 8 моль воды.
Окончательное уравнение реакции будет иметь вид
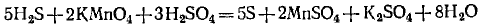
Правильность написания уравнения подтверждается подсчетом атомов одного элемента, например кислорода; в левой части их 2 
4+3 
4=20 и в правой 2 
4 + 4 + 8 = 20.
Переписываем уравнение в ионной форме:
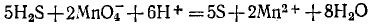
Известно, что правильно написанное уравнение реакции является выражением закона сохранения массы веществ. Поэтому число одних и тех же атомов в исходных веществах и продуктах реакции должно быть одинаковым. Должны сохраняться и заряды. Сумма зарядов исходных веществ всегда должна быть равна сумме зарядов продуктов реакции.
Метод полуреакций, или ионно-электронный метод
Как показывает само название, этот метод основан на составлении ионных уравнений для процесса окисления и процесса восстановления с последующим суммированием их в общее уравнение. В качестве примера составим уравнение той же реакции, которую использовали при объяснении метода электронного баланса (см. пример 3). При пропускании сероводорода H2S через подкисленный раствор перманганата калия КMnO4 малиновая окраска исчезает и раствор мутнеет. Опыт показывает, что помутнение раствора происходит в результате образования элементарной серы, т. е. протекания процесса:
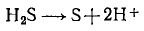
Эта схема уравнена по числу атомов. Для уравнивания по числу зарядов надо от левой части схемы отнять два электрона, после чего можно стрелку заменить на знак равенства:

Это первая полуреакция — процесс окисления восстановителя H2S.
Обесцвечивание раствора связано с переходом иона
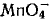
(он имеет малиновую окраску) в ион Mn2+ (практически бесцветный и лишь при большой концентрации имеет слабо-розовую окраску), что можно выразить схемой
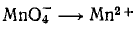
В кислом растворе кислород, входящий в состав ионов МnO4, вместе с ионами водорода в конечном итоге образует воду. Поэтому процесс перехода записываем так:
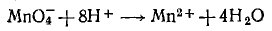
Чтобы стрелку заменить на знак равенства, надо уравнять и заряды. Поскольку исходные вещества имеют семь положительных зарядов (7+), а конечные —два положительных (2+), то для выполнения условия сохранения зарядов надо к левой части схемы прибавить пять электронов:
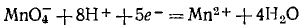
Для составления общего уравнения реакции надо уравнения полуреакций почленно сложить, предварительно уравняв числа отданных и полученных электронов. В этом случае по правилам нахождения наименьшего кратного определяют соответствующие множители, на которые умножаются уравнения полуреакций. Сокращенно запись проводится так:
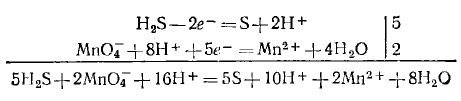
И сократив на 10H+, окончательно получим
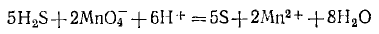
Проверяем правильность составленного в ионной форме уравнения: число атомов кислорода в левой части 8, в правой 8; число зарядов; в левой части (2-)+(6+)=4+, в правой 2(2+)=4+. Уравнение составлено правильно, так как атомы и заряды уравнены.
Методом полуреакций составляется уравнение реакции в ионной форме. Чтобы от него перейти к уравнению в молекулярной форме, поступаем так: в левой части конного уравнения к каждому аниону подбираем соответствующий катион, а к каждому катиону — анион. Затем те же ионы в таком же числе записываем в правую часть уравнения, после чего ноны объединяем в молекулы:
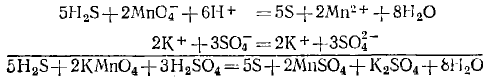
Таким образом, составление уравнений окислительно-восстановительных реакций с помощью метода полуреакций приводит к тому же результату, что и метод электронного баланса.
Сопоставим оба метода. Достоинство метода полуреакций по сравнению с методом электронного баланса в том, что в нем применяются не гипотетические ионы, а реально существующие. В самом деле, в растворе нет ионов
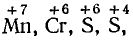
а есть ионы
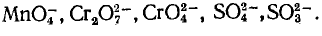
При методе полуреакций не нужно знать степень окисления атомов. Написание отдельных ионных уравнений полуреакций необходимо для понимания химических процессов в гальваническом элементе и при электролизе. При этом методе видна роль среды как активного участника всего процесса (см. § 7.4). Наконец, при использовании метода полуреакций не нужно знать все получающиеся вещества, они появляются в уравнении реакции при выводе его. Поэтому методу полуреакций следует отдать предпочтение и применять его при составлении уравнений всех окислительно-восстановительных реакций, протекающих в водных растворах.
Основные схемы окислительно-восстановительных реакций
Взаимодействие металлов с серной кислотой
Разбавленная серная кислота взаимодействует с металлами, как обычная минеральная кислота. Т.е. взаимодействует с металлами, которые расположены в ряду электрохимических напряжений до водорода. Окислителем здесь выступают ионы H+, которые восстанавливаются до молекулярного водорода H2. При этом металлы окисляются, как правило, до минимальнойстепени окисления.
Например:
Fe + H2SO4(разб) = FeSO4 + H2
Концентрированная серная кислота взаимодействует с металлами, стоящими в ряду напряжений как до, так и после водорода.
H2SO4 (конц) + металл = соль металла + продукт восстановления серы (SO2, S, H2S) + вода
При взаимодействии концентрированной серной кислоты с металлами образуются соль металла (в устойчивой степени окисления), вода и продукт восстановления серы — сернистый газ S+4O2, молекулярная сера S либо сероводород H2S-2, в зависимости от степени концентрации, активности металла, степени его измельчение, температуры и т.д. При взаимодействии концентрированной серной кислоты с металлами молекулярный водород не образуется!
Основные принципы взаимодействия концентрированной серной кислоты с металлами:
1.Концентрированная серная кислота пассивирует алюминий, хром, железо при комнатной температуре, либо на холоду;
2.Концентрированная серная кислотане взаимодействует сзолотом, платиной и палладием;
3. С неактивными металлами концентрированная серная кислота восстанавливается до оксида серы (IV).
Например, медь окисляется концентрированной серной кислотой:
Cu0 + 2H2S+6O4(конц) = Cu+2SO4 + S+4O2 + 2H2O
4. При взаимодействии с активными металлами и цинком концентрированная серная кислота образует серу S либо сероводород H2S2- (в зависимости от температуры, степени измельчения и активности металла).
Например, взаимодействие концентрированной серной кислоты с цинком:
8Na0+ 5H2S+6O4(конц) → 4Na2+SO4 + H2S—2 + 4H2O
Схема восстановления перманганатов
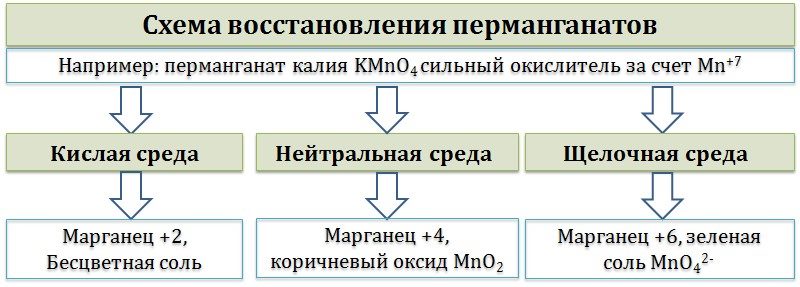
В составе перманганатов есть мощный окислитель — марганецв степени окисления +7. Соли марганца +7 окрашивают раствор в фиолетовый цвет.

Перманганаты, в зависимости от среды реакционного раствора, восстанавливаются по-разному.
В кислой среде восстановление происходит более глубоко, до Mn2+. Оксид марганца в степени окисления +2 проявляет основные свойства, поэтому в кислой средеобразуется соль. Соли марганца +2 бесцветны. В нейтральном растворемарганец восстанавливается до степени окисления +4, с образованием амфотерного оксида MnO2 — коричневогоосадка, нерастворимого в кислотах и щелочах. В щелочной среде марганец восстанавливается минимально — до ближайшей степени окисления +6. Соединения марганца +6 проявляют кислотные свойства, в щелочной среде образуют соли — манганаты. Манганаты придают раствору зеленую окраску.
Рассмотрим взаимодействие перманганата калия KMnO4 с сульфидом калия в кислой, нейтральной и щелочной средах. В этих реакциях продуктом окисления сульфид-иона является S0.
5 K2S + 2 KMnO4 + 8 H2SO4 = 5 S + 2 MnSO4 + 6 K2SO4 + 8 H2O,
3 K2S + 2 KMnO4 + 4 H2O = 2 MnO2↓ + 3 S↓ + 8 KOH,
Распространенной ошибкой в этой реакции является указание на взаимодействие серы и щелочи в продуктах реакции. Однако, сера взаимодействует с щелочью в довольно жестких условиях (повышенная температура), что не соответствует условиям этой реакции. При обычных условиях правильно будет указывать именно молекулярную серу и щелочь отдельно, а не продукты их взаимодействия.
K2S + 2 KMnO4 –(KOH)= 2 K2MnO4 + S↓
При составлении этой реакции также возникают трудности. Дело в том, что в данном случае написание молекулы среды (КОН или другая щелочь) в реагентах не требуется для уравнивания реакции. Щелочь принимает участие в реакции, и определяет продукт восстановления перманганата калия, но реагенты и продукты уравниваются и без ее участия. Этот, казалось бы, парадокс легко разрешим, если вспомнить, что химическая реакция — это всего лишь условная запись, которая не указывает на каждый происходящий процесс, а всего лишь является отображением суммы всех процессов. Как определить это самостоятельно? Если действовать по классической схеме — баланс-балансовые коэффициенты-уравнивание металла, то вы увидите, что металлы уравниваются балансовыми коэффициентами, и наличие щелочи в левой части уравнения реакции будет лишним.
Перманганаты окисляют:
- неметаллыс отрицательной степенью окисления до простых веществ (со степенью окисления 0), исключения— фосфор, мышьяк — до +5;
- неметаллыс промежуточной степенью окисления до высшей степени окисления;
- активные металлыиз простых веществ (ст.окисления 0) до соединений со стабильной положительной степенью окисления металла.
KMnO4 + неМе (низшая с.о.) = неМе0 + другие продукты
KMnO4 + неМе (промежуточная с.о.) = неМе(высшая с.о.) + др. продукты
KMnO4 + Ме0 = Ме (стабильная с.о.) + др. продукты
KMnO4 + P-3, As-3= P+5, As+5 + др. продукты
Азотистая кислота и нитриты
При взаимодействии с более сильными окислителями азот повышает степень окисления до +5 и превращается либо в азотную кислоту из азотистой, либо в нитрат-анион из нитрит-аниона: 5NaNO2 + 2KMnO4 + 3H2SO4 = 5NaNO3 + 2MnSO4 + K2SO4 + 3H2O.
При взаимодействии с сильными восстановителями обычно происходит восстановление до NO (иногда до других соединений азота в более низких степенях окисления): 2HNO2 + 2HI = 2NO + I2 + 2H2O.
Для удобства мы собрали представителей типичных окислителей и восстановителей в одну схему.

Пероксид водорода
Атом кислорода в пероксиде водорода находится в промежуточной степени окисления –1, и в присутствии восстановителей может понижать степень окисления до –2: 4H2O2 + PbS = PbSO4 + 4H2O.
Атом кислорода в пероксиде водорода находится в промежуточной степени окисления –1, и в присутствии окислителей может повышать степень окисления до 0: 3H2O2 + 2KMnO4 = 3O2 + 2MnO2 + 2KOH + 2H2O.
Окислительные свойства азотной кислоты
Азотная кислота HNO3 при взаимодействии с металлами практически никогда не образует водород, в отличие от большинства минеральных кислот.
Это связано с тем, что в составе кислоты есть очень сильный окислитель — азот в степени окисления +5. При взаимодействии с восстановителями — металлами образуются различные продукты восстановления азота.
Азотная кислота + металл = соль металла + продукт восстановления азота + H2O
Азотная кислота при восстановлении может переходить в оксид азота (IV) NO2 (N+4); оксид азота (II) NO (N+2); оксид азота (I) N2O («веселящий газ»); молекулярный азот N2; нитрат аммония NH4NO3. Как правило, образуется смесь продуктов с преобладанием одного из них. Азот восстанавливается при этом до степеней окисления от +4 до −3. Глубина восстановления зависит в первую очередь от природы восстановителя и от концентрации азотной кислоты. При этом работает правило: чем меньше концентрация кислоты и выше активность металла, тем больше электронов получает азот, и тем более восстановленные продукты образуются.
Некоторые закономерности позволят верно определять основной продукт восстановления металлами азотной кислоты в реакции:
- при действии очень разбавленной азотной кислоты на металлы образуется, как правило, нитрат аммония NH4NO3;
Например, взаимодействие цинка с очень разбавленной азотной кислотой:
4Zn + 10HNO3 = 4Zn(NO3)2 + NH4NO3 + 3H2O
- концентрированная азотная кислота на холодепассивирует некоторые металлы — хром Cr, алюминий Al и железо Fe. При нагревании или разбавлении раствора реакция идет;
пассивация металлов — это перевод поверхности металла в неактивное состояние за счет образования на поверхности металла тонких слоев инертных соединений, в данном случае преимущественно оксидов металлов, которые не реагируют с концентрированной азотной кислотой
- азотная кислота не реагирует с металлами платиновой подгруппы — золотом Au, платинойPt, и палладием Pd;
- при взаимодействии концентрированной кислоты с неактивными металлами и металлами средней активности азотная кислота восстанавливается до оксида азота (IV)NO2;
Например, окисление меди концентрированной азотной кислотой:
Cu+ 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
- при взаимодействии концентрированной азотной кислоты с активными металлами образуется оксид азота(I) N2O;
Например, окисление натрия концентрированной азотной кислотой:
8Na+ 10HNO3 = 8NaNO3 + N2O + 5H2O
- при взаимодействии разбавленной азотной кислоты с неактивными металлами (в ряду активности правее водорода) кислота восстанавливается до оксида азота (II) NO;
- при взаимодействии разбавленной азотной кислоты с металлами средней активности образуется либо оксид азота (II) NO, либо оксид азота N2O, либо молекулярный азот N2 — в зависимости от дополнительных факторов (активность металла, степень измельчения металла, степень разбавления кислоты, температура).
- при взаимодействии разбавленной азотной кислоты с активными металлами образуется молекулярный азот N2.
Для приближенного определения продуктов восстановления азотной кислоты при взаимодействии с разными металлами я предлагаю воспользоваться принципом маятника. Основные факторы, смещающие положение маятника: концентрация кислоты и активность металла. Для упрощения используем 3 типа концентраций кислоты: концентрированная (больше 30%), разбавленная (30% или меньше), очень разбавленная (меньше 5%). Металлы по активности разделим на активные (до алюминия), средней активности (от алюминия до водорода) и неактивные (после водорода). Продукты восстановления азотной кислоты располагаем в порядке убывания степени окисления:
NO2; NO; N2O; N2; NH4NO3
Чем активнее металл, тем больше мы смещаемся вправо. Чем больше концентрация или меньше степень разбавления кислоты, тем больше мы смещаемся влево.
Например, взаимодействуют концентрированная кислота и неактивный металл медь Cu. Следовательно, смещаемся в крайнее левое положение, образуется оксид азота (IV), нитрат меди и вода.
Схема восстановления хроматов/бихроматов
Особенностью хрома с валентностью VI является то, что он образует 2 типа солей в водных растворах: хроматы и бихроматы, в зависимости от среды раствора. Хроматы активных металлов (например, K2CrO4) — это соли, которые устойчивы в щелочнойсреде. Дихроматы (бихроматы) активных металлов (например, K2Cr2O7) — соли, устойчивые в кислой среде.
Восстанавливаются соединения хрома (VI) до соединений хрома (III). Соединения хрома Cr+3 — амфотерные, и в зависимости от среды раствора они существуют в растворе в различных формах: в кислой среде в виде солей(амфотерные соединения при взаимодействии с кислотами образуют соли), в нейтральной среде — нерастворимый амфотерный гидроксид хрома (III) Cr(OH)3, и в щелочной среде соединения хрома (III) образуют комплексную соль, например, гексагидроксохромат (III) калия K3[Cr(OH)6].

Соединения хрома VI окисляют:
- неметаллыв отрицательной степени окисления до простых веществ (со степенью окисления 0), исключения— фосфор, мышьяк – до +5;
- неметаллыв промежуточной степени окисления до высшей степени окисления;
- активные металлыиз простых веществ (ст.окисления 0) до соединений со стабильной положительной степенью окисления металла.
Хромат/бихромат + неМе (отрицательная с.о.) = неМе0 + другие продукты
Хромат/бихромат + неМе (промежуточная положительная с.о.) = неМе(высшая с.о.) + др. продукты
Хромат/бихромат + Ме0 = Ме (стабильная с.о.) + др. продукты
Хромат/бихромат + P, As (отрицательная с.о.) = P, As+5 + другие продукты